De l’observation clinique à l’hypothèse neurophysiologique
La présente page propose une lecture macroscopique et neurophysiologique des effets observés lors de l’application du protocole de Pression Focale®, en particulier dans le cadre de la prise en charge des douleurs chroniques et persistantes.
Elle s’appuie sur des observations cliniques répétées, rapportant un effet antalgique rapide, parfois immédiat, associé à une amélioration transitoire de la tolérance mécanique des tissus traités.
Ces effets cliniques ne peuvent être attribués à un mécanisme unique. Les modèles contemporains de la douleur soulignent au contraire le caractère multifactoriel de la modulation nociceptive, impliquant des interactions complexes entre mécanismes périphériques, spinaux et centraux, ainsi que des phénomènes de neuroplasticité dépendants de l’expérience sensorielle.
La Pression Focale® repose sur une stimulation mécanique précise, localisée et contrôlée, susceptible d’interagir avec ces différents niveaux de régulation de la douleur. Le cadre théorique présenté ici vise à articuler les observations cliniques avec les connaissances actuelles en neurophysiologie de la douleur, sans prétendre à une relation causale démontrée.
Comme pour la page microscopique, ce contenu s’inscrit dans une démarche hypothétique et explicative, destinée à soutenir la réflexion clinique et à préparer des travaux de recherche clinique structurés, en lien avec des équipes spécialisées en recherche interventionnelle et observationnelle.
Effet antalgique immédiat et modulation du signal nociceptif
L’un des éléments cliniques fréquemment rapportés lors de l’application du protocole de Pression Focale® est l’apparition d’un effet antalgique rapide, parfois immédiat. Ce phénomène suggère une modulation précoce du signal nociceptif, survenant avant toute modification tissulaire macroscopique identifiable.
Cette analgésie initiale permet une diminution transitoire du bruit nociceptif, facilitant l’examen clinique et l’identification plus fine des zones présentant une pertinence mécanique ou neuro-sensorielle. Elle constitue ainsi un élément fonctionnel important dans l’orientation et l’ajustement de la prise en charge.
Stimulation mécanique focalisée
↓
Effet antalgique rapide
(modulation neurophysiologique)
↓
Diminution du bruit nociceptif
↓
Adaptations secondaires
(tissulaires, neuroplastiques, fonctionnelles)
Schéma 1 — Chronologie conceptuelle des effets observés.
La stimulation mécanique focalisée est associée à un effet antalgique rapide, principalement attribuable à des mécanismes de modulation neurophysiologique. Cette analgésie initiale précède d’éventuelles adaptations secondaires, impliquant des mécanismes périphériques et centraux, dont la temporalité et l’importance relative peuvent varier selon les situations cliniques.
Théorie du Gate Control et afférences mécanosensibles
La théorie du Gate Control, proposée par Melzack et Wall, suggère que l’activation des fibres nerveuses de gros diamètre (Aβ), sensibles aux stimuli mécaniques, peut inhiber la transmission des afférences nociceptives au niveau spinal. Selon ce modèle, la balance entre les informations sensorielles non nociceptives et nociceptives conditionne l’intensité du signal douloureux transmis aux centres supérieurs.
Dans ce cadre, une stimulation mécanique précise et localisée est susceptible de moduler temporairement la perception douloureuse en favorisant l’activation des afférences mécanosensibles, contribuant ainsi à une diminution du signal nociceptif ascendant. Ce mécanisme est classiquement décrit comme l’un des fondements neurophysiologiques de l’analgésie induite par certaines stimulations mécaniques.
Melzack R et Wall PD ont formalisé ce modèle dans leur article fondateur, établissant un cadre conceptuel majeur pour la compréhension de la modulation de la douleur au niveau spinal (Melzack & Wall, 1965 — Science, PMID: 5320816).
[Lien PubMed]
Ce modèle, bien que simplificateur, constitue toujours un cadre conceptuel majeur de la modulation segmentaire de la douleur, aujourd’hui intégré dans des modèles plus complexes de contrôle central.
Contrôle Inhibiteur Diffus Nociceptif (CIDN)
Une stimulation mécanique localisée, d’intensité suffisante mais contrôlée, est susceptible d’activer les systèmes inhibiteurs descendants de la douleur. Ce mécanisme est décrit dans le cadre du Contrôle Inhibiteur Diffus Nociceptif (CIDN), également désigné sous le terme de Diffuse Noxious Inhibitory Controls (DNIC) dans la littérature anglo-saxonne.
L’activation de ces voies inhibitrices repose sur l’implication de structures supraspinales, notamment au niveau du tronc cérébral, et s’accompagne de la libération de médiateurs inhibiteurs tels que les opioïdes endogènes, mais également de monoamines, en particulier la sérotonine et la noradrénaline. Ces neurotransmetteurs participent à la modulation descendante de la transmission nociceptive au niveau spinal.
Ce mécanisme peut contribuer à une analgésie parfois disproportionnée par rapport à la surface stimulée, traduisant une modulation centrale du signal nociceptif plutôt qu’un simple effet local. Ce phénomène est classiquement résumé par l’expression « la douleur qui inhibe la douleur », utilisée ici à des fins descriptives.
Le CIDN doit être considéré comme un facilitateur neurophysiologique, susceptible de participer à l’effet antalgique initial observé lors de certaines stimulations mécaniques focalisées, sans constituer à lui seul un mécanisme explicatif unique des effets cliniques associés.
Le Bars D. et al. ont formalisé le concept de DNIC en décrivant l’activation de voies inhibitrices descendantes modulant l’activité des neurones nociceptifs spinaux (Le Bars et al., 1979 — Pain, PMID: 460935).
[Lien PubMed]
📐Schéma 2 — Voies descendantes inhibitrices et modulation centrale de la nociception.
Centres supraspinaux
(tronc cérébral, structures impliquées
dans la modulation de la douleur)
↓
Voies descendantes inhibitrices
(systèmes opioïdes endogènes,
réseaux inhibiteurs)
↓
Moelle épinière
(modulation de la transmission nociceptive)
↓
Signal nociceptif ascendant
(modulé)
Schéma 2 — Voies descendantes inhibitrices et modulation centrale de la nociception.
Certaines stimulations mécaniques peuvent s’inscrire dans des mécanismes de modulation centrale de la douleur, impliquant l’activation de voies inhibitrices descendantes. Ces voies contribuent à moduler la transmission des signaux nociceptifs au niveau spinal, sans constituer un mécanisme exclusif ni systématique des effets antalgiques observés.
Réduction du bruit nociceptif périphérique
La douleur chronique est fréquemment associée à une hyperexcitabilité périphérique, entretenue par une inflammation de bas grade, une hypoxie locale et des contraintes mécaniques anormales au niveau des tissus.
Dans ce contexte, une stimulation mécanique ciblée pourrait modifier l’environnement local des nocicepteurs, contribuant à une diminution du bruit nociceptif périphérique et à une amélioration transitoire du rapport signal/bruit sensoriel.
Modulation inflammatoire et microcirculation
Les stimulations mécaniques peuvent influencer la microcirculation locale et la dynamique inflammatoire. Plutôt qu’une inflammation aiguë, il est plausible qu’une stimulation focalisée participe à une modulation de la réponse inflammatoire de bas grade, créant un environnement plus favorable aux processus adaptatifs et réparateurs.
Toute hypothèse de néovascularisation doit être considérée comme exploratoire.
Neuroplasticité et intégration somatotopique
Les douleurs chroniques s’accompagnent fréquemment d’altérations de la représentation corticale des régions corporelles concernées. Ces modifications se traduisent par une diminution de la discrimination sensorielle, une désorganisation ou une expansion des cartes somatotopiques, et une persistance du signal nociceptif indépendamment de la stimulation périphérique initiale.
Ces phénomènes sont décrits dans le cadre des modèles de neuroplasticité maladaptative, selon lesquels une expérience douloureuse prolongée peut induire des réorganisations durables du système nerveux central participant à la chronicisation de la douleur.
Dans cette perspective, certaines stimulations sensorielles précises et répétées sont susceptibles d’améliorer la qualité du signal afférent transmis au système nerveux central et de favoriser une réintégration somatotopique plus cohérente. Cette hypothèse s’inscrit dans les modèles contemporains de neuroplasticité dépendante de l’expérience, où la spécificité, la précision et la pertinence des afférences sensorielles jouent un rôle déterminant dans les processus de réorganisation corticale.
Flor H., Nikolajsen L. et Staehelin Jensen T. ont décrit la douleur de membre fantôme comme un exemple paradigmatique de plasticité maladaptative du système nerveux central, en mettant en évidence le lien entre réorganisation corticale et persistance de la douleur (Flor et al., 2006 — Nat Rev Neurosci, PMID: 17053811).
[Lien PubMed]
Plus récemment, Kuner R. et Flor H. ont proposé une synthèse des mécanismes de plasticité structurelle et fonctionnelle impliqués dans les douleurs chroniques, soulignant que ces réorganisations sont dynamiques, dépendantes de l’expérience sensorielle et potentiellement modulables dans certaines conditions expérimentales (Kuner & Flor, 2017 — Nat Rev Neurosci, PMID: 27974843).
[Lien PubMed]
📐Schéma 3 — Représentation corticale altérée versus représentation plus discriminée.
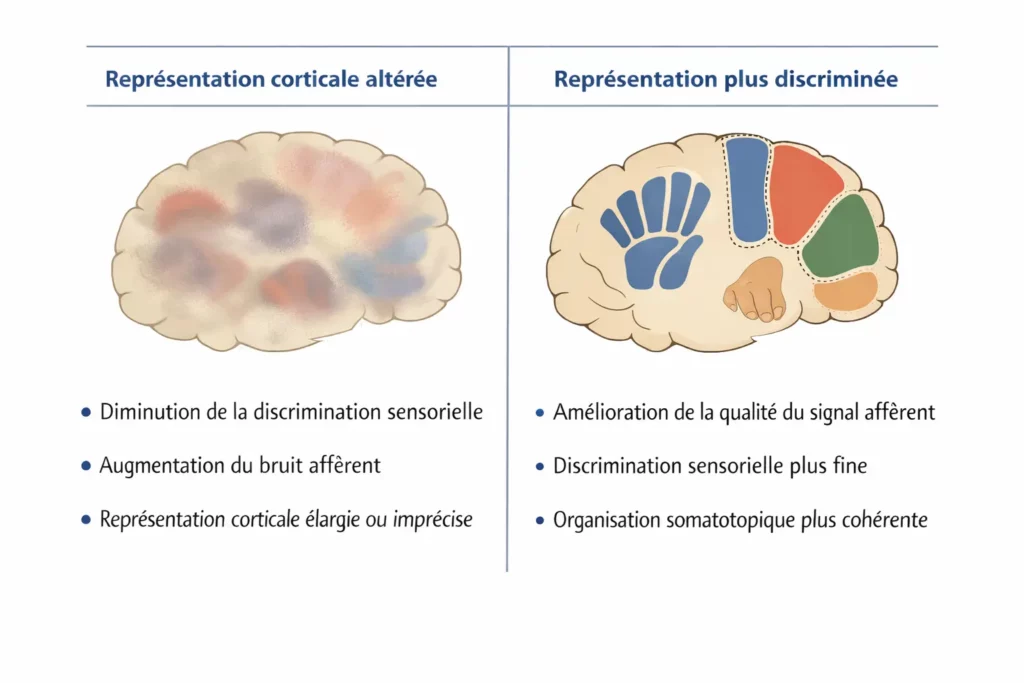
Schéma 3 — Représentation corticale altérée versus représentation plus discriminée.
Les douleurs chroniques sont associées à des altérations de la représentation somatotopique, caractérisées par une diminution de la discrimination sensorielle et une augmentation du bruit afférent. Certaines stimulations sensorielles précises et répétées peuvent s’inscrire dans des processus de neuroplasticité dépendants de l’expérience, favorisant une organisation corticale plus cohérente, sans préjuger d’un effet systématique ou causal.
Synthèse des mécanismes macroscopiques
Les effets observés lors de la Pression Focale® résultent probablement de l’interaction de mécanismes neurophysiologiques multiples, agissant à différents niveaux du système nerveux et périphérique. Cette lecture multifactorielle reflète la complexité de la douleur chronique et justifie une approche clinique raisonnée et intégrative.
Il convient de souligner que l’importance relative de chacun de ces mécanismes peut varier selon les contextes cliniques, les tissus concernés et l’histoire douloureuse du patient.
Cette lecture macroscopique complète le cadre théorique microscopique de la Pression Focale®.
