Positionnement scientifique et statut du modèle proposé
La présente page expose le cadre théorique microscopique sur lequel s’appuie le protocole de Pression Focale®, en s’inscrivant dans les champs contemporains de la mécanobiologie et de la mécanotransduction cellulaire.
Elle vise à proposer un modèle explicatif cohérent, fondé sur les données actuelles de la biologie cellulaire, permettant de relier une stimulation mécanique ciblée à des réponses biologiques observables au sein des tissus conjonctifs.
La littérature scientifique a largement démontré que les cellules ne sont pas de simples structures passives, mais qu’elles sont capables de percevoir, transmettre et traduire les contraintes mécaniques de leur environnement en signaux biochimiques influençant leur comportement, leur organisation et leur fonction. Les fibroblastes, en particulier, jouent un rôle central dans cette dynamique adaptative, en lien étroit avec la matrice extracellulaire et le cytosquelette.
Le cadre présenté ici ne constitue pas une preuve d’efficacité clinique, mais une hypothèse mécanobiologique structurée, destinée à éclairer la pratique manuelle et à servir de socle conceptuel à des travaux de recherche clinique de type observationnel (case series, études pilotes).
Il s’inscrit dans une démarche de pratique raisonnée, ouverte à la discussion scientifique, à la réfutation et à l’évolution des modèles en fonction de l’avancée des connaissances.
La mécanotransduction : conversion du signal mécanique en réponse biologique
Les tissus conjonctifs ne constituent pas de simples structures de soutien passives. Les travaux en mécanobiologie ont mis en évidence que les cellules sont capables de percevoir les contraintes mécaniques, de les transmettre à travers leur architecture interne et de les traduire en réponses biologiques spécifiques. Ce processus, désigné sous le terme de mécanotransduction, joue un rôle central dans l’homéostasie tissulaire, l’adaptation mécanique et les phénomènes de réparation.
Une stimulation mécanique ciblée, lorsqu’elle est appliquée de manière contrôlée, peut modifier l’environnement mécanique local de la matrice extracellulaire. Cette modification est perçue par les cellules via des complexes d’adhésion reliant la matrice au cytosquelette, entraînant des cascades de signalisation intracellulaire susceptibles d’influencer l’expression génique, la synthèse de protéines matricielles et l’organisation structurale du tissu.
Ingber DE a décrit un cadre mécanobiologique, reposant notamment sur le modèle de la tenségrité biologique, selon lequel les cellules sont capables de répondre aux contraintes mécaniques en transmettant les forces de la matrice extracellulaire à travers le cytosquelette jusqu’au noyau cellulaire (Ingber, 2003 — Ann Med, PMID: 14708967).
[Lien PubMed]
Dans la continuité de ces travaux, Jaalouk DE et Lammerding J. ont ont décrit comment des altérations de la transmission des forces mécaniques et de la signalisation associée sont impliquées dans des états pathologiques, soulignant le rôle central de la mécanotransduction dans le maintien de la fonction cellulaire (Jaalouk & Lammerding, 2009 — Nat Rev Mol Cell Biol, PMID: 19197333).
[Lien PubMed]
📐 Schéma 1 conceptuel de la mécanotransduction : matrice extracellulaire → intégrines → cytosquelette → noyau.
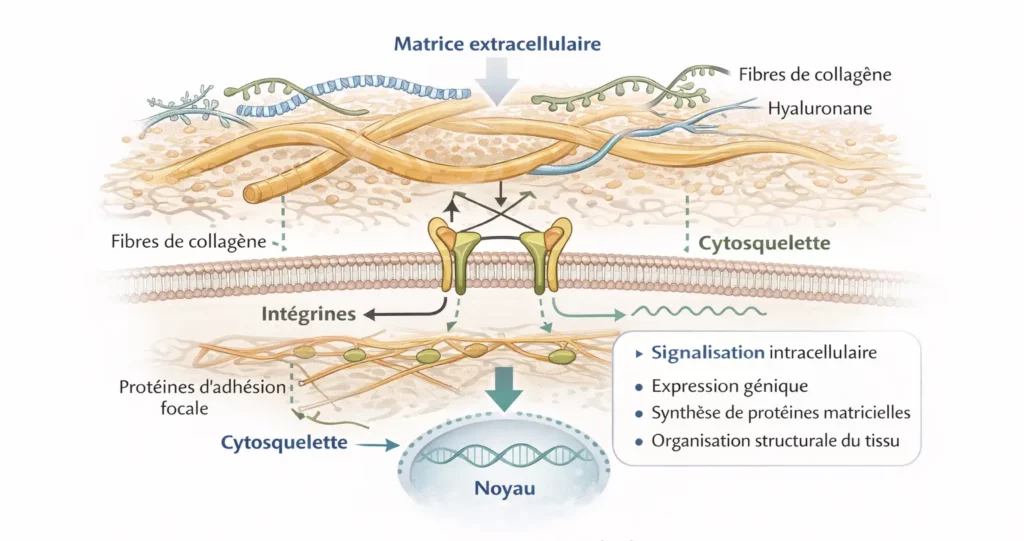
Schéma 1 — Mécanotransduction : conversion d’un signal mécanique en réponse biologique.
Illustration conceptuelle du processus par lequel une contrainte mécanique appliquée à la matrice extracellulaire peut être transmise à la cellule via les intégrines et le cytosquelette, jusqu’au noyau cellulaire. Cette transmission mécanique est susceptible d’induire des cascades de signalisation intracellulaire influençant l’expression génique et l’organisation structurale du tissu. Ce schéma ne constitue pas une démonstration causale, mais une représentation théorique issue des modèles actuels de mécanobiologie.
Modèle de la tenségrité : transmission des contraintes de la matrice au noyau
Le modèle de la tenségrité biologique, développé notamment par Donald Ingber, propose que les tissus vivants fonctionnent comme des systèmes architecturaux précontraints, dans lesquels les forces mécaniques sont distribuées à travers un réseau continu reliant la matrice extracellulaire, le cytosquelette et le noyau cellulaire. Ce cadre conceptuel suggère que la stabilité et la fonction des tissus reposent sur un équilibre dynamique entre forces de tension et de compression.
Dans cette perspective, une contrainte mécanique appliquée localement n’est pas dissipée uniquement au point d’application, mais peut être transmise à distance à travers les réseaux de tension du tissu. Ce modèle soutient l’hypothèse selon laquelle une stimulation mécanique précise et focalisée est susceptible d’influencer l’équilibre mécanique global d’un tissu, voire de structures interconnectées, sans nécessiter une action extensive ou diffuse.
Ingber DE a formalisé le modèle de la tenségrité biologique, montrant comment les forces mécaniques appliquées à la matrice extracellulaire peuvent être transmises à travers le cytosquelette jusqu’au noyau cellulaire, influençant la signalisation intracellulaire et l’expression génique (Ingber, 2008 — J Bodyw Mov Ther, PMID: 19083675).
[Lien PubMed]
Dans la continuité de ces travaux, Wang N, Butler JP et Ingber DE ont décrit le comportement mécanique des cellules vivantes, en démontrant que le cytosquelette joue un rôle central dans la transmission et l’intégration des contraintes mécaniques à l’échelle cellulaire. Leurs expériences ont montré que les intégrines agissent comme des mécanorécepteurs et que les forces appliquées à la surface cellulaire peuvent être transmises à travers un cytosquelette intégré sous tension (Wang et al., 1993 — Science, PMID: 7684161).
[Lien PubMed]
📐 Schéma 2 de tenségrité cellulaire montrant la continuité des forces de la matrice au noyau.
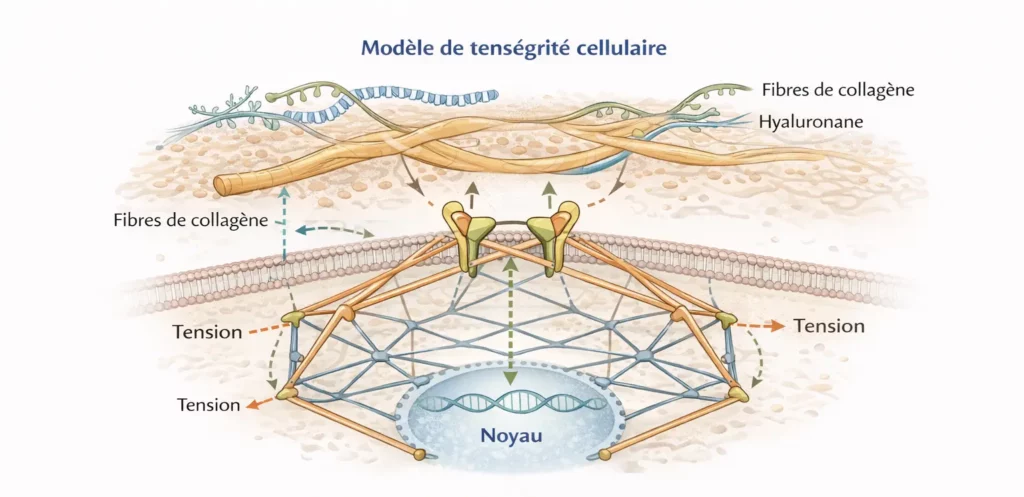
Schéma 2 — Modèle de la tenségrité cellulaire et continuité des forces mécaniques.
Représentation conceptuelle du modèle de la tenségrité appliqué à la cellule, dans lequel les forces mécaniques exercées sur la matrice extracellulaire sont distribuées à travers un réseau continu reliant les intégrines, le cytosquelette et le noyau cellulaire. Selon ce modèle, les contraintes mécaniques ne sont pas dissipées localement mais intégrées à l’architecture cellulaire globale. Ce schéma illustre un cadre théorique issu des travaux en mécanobiologie et ne constitue pas une démonstration causale des effets cliniques observés.
Fibroblastes et cellules mécanosensibles du tissu conjonctif
Les fibroblastes constituent une population cellulaire clé du tissu conjonctif. Loin d’être de simples producteurs de collagène, ils jouent un rôle actif dans la perception des contraintes mécaniques et l’adaptation tissulaire. Ces cellules sont capables de modifier leur forme, leur tension interne et leur organisation cytosquelettique en réponse à des stimulations mécaniques spécifiques, participant ainsi à la régulation dynamique des propriétés mécaniques du tissu.
Des travaux expérimentaux in vitro ont mis en évidence que des stimulations mécaniques peuvent induire un remodelage rapide du cytosquelette des fibroblastes, observable en quelques minutes, suggérant une capacité d’adaptation dynamique du tissu conjonctif aux contraintes appliquées. Ces observations apportent un rationnel biologique cohérent aux modifications palpatoires et mécaniques rapportées lors de certaines interventions manuelles.
Langevin HM et al. ont montré, dans des modèles expérimentaux, que le remodelage du cytosquelette des fibroblastes contribue directement à la tension du tissu conjonctif, soulignant le rôle central de ces cellules dans la réponse mécanique des tissus (Langevin et al., 2011 — J Cell Physiol, PMID: 20945345).
[Lien PubMed]
Dans une perspective plus large, Tomasek JJ et al. ont décrit le rôle des fibroblastes et des myofibroblastes dans la mécano-régulation du remodelage conjonctif, ont décrit le rôle des fibroblastes et des myofibroblastes dans la mécano-régulation du remodelage conjonctif, mettant en évidence l’influence déterminante des contraintes mécaniques sur le comportement cellulaire et l’organisation tissulaire, notamment dans les processus de cicatrisation normale et pathologique (Tomasek et al., 2002 — Nat Rev Mol Cell Biol, PMID: 11988769).
[Lien PubMed]
📐 Schéma 3 illustrant le remodelage cytosquelettique des fibroblastes en réponse à une contrainte mécanique.
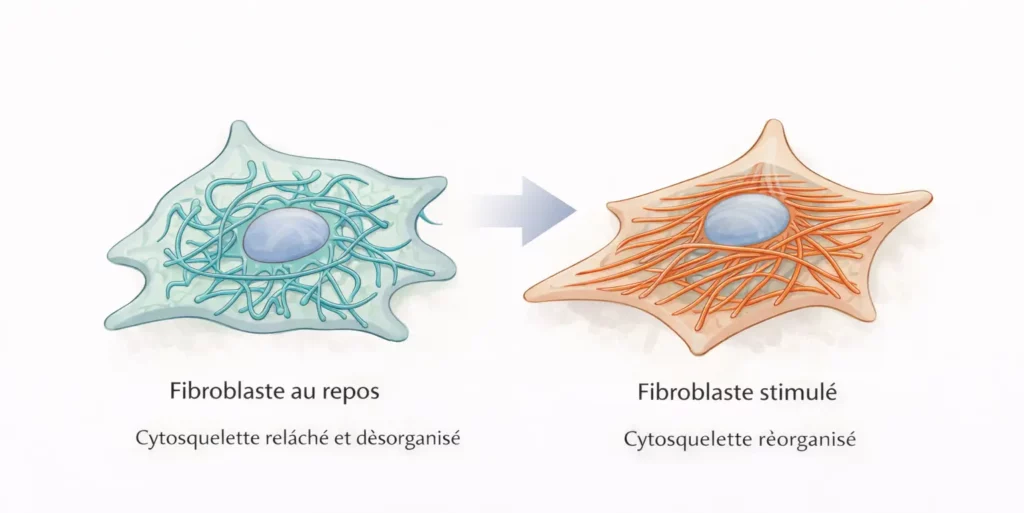
Schéma 3 — Remodelage cytosquelettique des fibroblastes en réponse à une contrainte mécanique.
Illustration conceptuelle montrant la capacité des fibroblastes à réorganiser leur cytosquelette, notamment actinique, en réponse à une stimulation mécanique. Les travaux expérimentaux ont mis en évidence que ces cellules peuvent modifier rapidement leur forme, leur tension interne et l’orientation de leurs fibres cytosquelettiques, traduisant une adaptation dynamique du tissu conjonctif aux contraintes appliquées.
Ce schéma s’inscrit dans un cadre mécanobiologique issu de la littérature scientifique et ne constitue pas une démonstration causale ni une preuve d’efficacité clinique.
Densification de la matrice extracellulaire et implications nociceptives
Les travaux récents sur le fascia ont mis en évidence que certaines douleurs chroniques sont associées à une densification de la matrice extracellulaire, notamment liée à une accumulation d’hyaluronane et à une altération des capacités de glissement entre les plans tissulaires. Cette densification modifie les propriétés viscoélastiques locales du tissu et peut créer un environnement mécanique défavorable pour les structures nerveuses adjacentes.
Dans ce contexte, la densification fasciale est susceptible d’augmenter les contraintes mécaniques exercées sur les terminaisons nerveuses, contribuant ainsi au maintien d’un signal nociceptif périphérique. Ce mécanisme est proposé comme l’un des facteurs impliqués dans la persistance des douleurs myofasciales, indépendamment de toute lésion structurale macroscopique identifiable.
Stecco A et al. ont décrit les composants fasciaux impliqués dans le syndrome douloureux myofascial, mettant en évidence le rôle de la matrice extracellulaire et de sa densification dans la genèse et l’entretien de la douleur (Stecco et al., 2013 — Curr Pain Headache Rep, PMID: 23801005).
[Lien PubMed]
Dans la continuité de ces travaux, Pavan PG et al. ont distingué les concepts de densification et de fibrose fasciale, en soulignant le rôle central de l’hyaluronane dans les modifications mécaniques du fascia et leurs implications fonctionnelles (Pavan et al., 2014 — Surg Radiol Anat, PMID: 25063495).
[Lien PubMed]
Dans cette perspective, une stimulation mécanique ciblée, appliquée de manière contrôlée, pourrait contribuer à modifier localement les propriétés viscoélastiques de la matrice, influençant ainsi la contrainte exercée sur les terminaisons nerveuses et participant à la modulation de la nociception périphérique. Cette hypothèse s’inscrit dans un cadre explicatif et nécessite une validation expérimentale spécifique.
Précision sur la densification fasciale
Les travaux de Stecco et collaborateurs suggèrent que la densification fasciale est principalement liée à des modifications des propriétés viscoélastiques de la substance fondamentale, et en particulier de l’hyaluronane. Selon ces modèles, des variations de température locale, de contraintes mécaniques ou de forces de cisaillement peuvent influencer l’organisation moléculaire de l’hyaluronane, favorisant un passage d’un état plus visqueux (« gel-like ») à un état plus fluide (« sol-like »).
Cette hypothèse permet d’envisager la densification non comme une accumulation fibreuse irréversible, mais comme un état mécanique potentiellement modulable de la matrice extracellulaire, distinct des processus de fibrose collagénique.
📐 Schéma 4 — Schéma conceptuel illustrant une matrice extracellulaire densifiée (augmentation de la viscosité de la substance fondamentale) comparée à une matrice plus fluide, distincte des processus de fibrose collagénique.
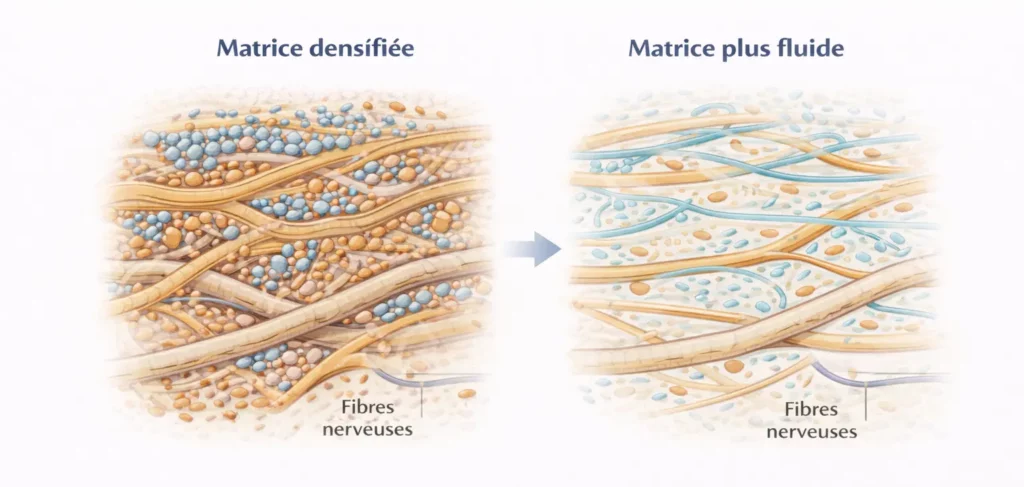
Schéma 4 — Densification de la matrice extracellulaire et variations de ses propriétés viscoélastiques
Illustration conceptuelle comparant une matrice extracellulaire densifiée, caractérisée par une accumulation d’hyaluronane et une diminution des capacités de glissement intertissulaire, à une matrice présentant une fluidité relative plus élevée, associée à des propriétés viscoélastiques plus favorables.
La densification matricielle est susceptible de modifier l’environnement mécanique local ainsi que les contraintes exercées sur les structures cellulaires et nerveuses adjacentes.
Ce schéma propose une représentation théorique des états tissulaires décrits dans la littérature et ne constitue ni une normalisation attendue ni une démonstration causale des effets cliniques observés.
Hypothèses mécanobiologiques et limites
L’ensemble de ces éléments soutient l’hypothèse selon laquelle une stimulation mécanique focalisée, appliquée dans des conditions contrôlées, pourrait influencer l’adaptation tissulaire à travers des mécanismes mécanobiologiques identifiés dans la littérature.
Ce cadre microscopique constitue une base conceptuelle explicative, et non une démonstration causale. Il a vocation à orienter des travaux de recherche clinique de type observationnel ou expérimental, et à structurer l’interprétation des observations issues de la pratique clinique.
Cette lecture microscopique complète le cadre théorique macroscopique de la Pression Focale®.
